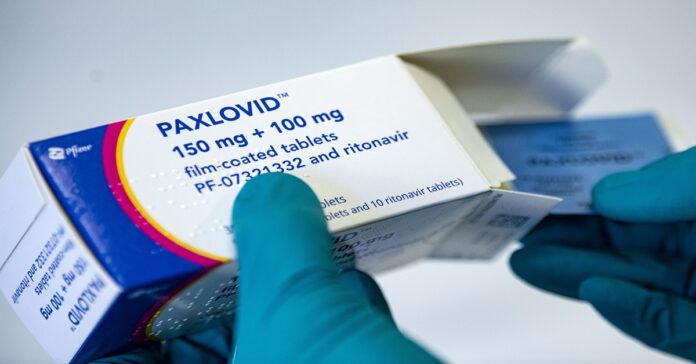
- Tratamiento de la COVID-19 en adultos que no requieren oxígeno suplementario.
- A este tratamiento se suma el Molnupiravir 200 mg cápsulas de la empresa Merck Sharp & Dohme Corp.
Redacción- El Ministerio de Salud autorizó el uso de emergencia para el medicamento Paxlovid 150/100 mg cápsulas de la compañía Pfizer, la cual ya fue notificada y la faculta para su venta a nivel nacional.
El Paxlovid está indicado para el tratamiento de la COVID-19 en adultos que no requieren oxígeno suplementario y que tienen alto riesgo de progresión a COVID-19 de severo – grave.
La dosis recomendada en pacientes adultos es de 300 mg de nirmatrelvir (dos comprimidos de 150 mg) con 100 mg de ritonavir (un comprimido de 100 mg), tomados simultáneamente por vía oral dos veces al día durante 5 días con o sin alimentos.
LEA TAMBIÉN: Autorizan venta en el país de tratamiento contra el Covid-19
Asimismo, se debe administrar lo antes posible después de haber dado positivo en la prueba viral directa para el SARS-CoV-2 y dentro de los primeros 5 días siguientes a la aparición de los síntomas.
La autorización de uso se brinda basada en la Resolución Administrativa MS-DM-RM-1363-2022 publicada el 24 de enero de este año, donde se establecen los requisitos para obtener una Autorización de Uso e Importación de los medicamentos para tratar la COVID-19, basado en el reconocimiento de la Autorización de comercialización o Autorización de uso de emergencia de Autoridades Reguladoras Estrictas o de medicamentos recomendados por la Organización Mundial de la Salud.
Como parte de la autorización la empresa Pfizer Zona Franca S.A. debe asegurar registros de la distribución del medicamento (es decir, números de lotes, cantidad, fecha y destino), así como presentar informes mensuales de posibles eventos adversos o de seguridad.
El Ministerio de Salud afirma que no tienen relación con los tiempos de importación del medicamento, ni con los precios que tendrá este en el país.
A este tratamiento se suma el Molnupiravir 200 mg cápsulas de la empresa Merck Sharp & Dohme Corp, el cual fue autorizado el pasado 23 de febrero del 2022 mediante la resolución MS-DRPIS-AUE-M-01-2022.